您當前的(de)位置: 首頁 - 新聞資訊 - 詳細內(nèi)容
概要:脂質納米顆粒(LNPs)是一(yī)種具有(yǒu)均勻脂質核的(de)脂囊泡,被廣泛應用于小分子(zǐ)藥物和(hé)核酸輸送,最近因為(wèi)在COVID-19 mRNA疫苗遞送平台取得的(de)顯著成功引起了廣泛的(de)關注。然而,mRNA誘導的(de)短(duǎn)暫蛋白表達的(de)應用并不僅僅用于傳染性疾病的(de)疫苗領域,也為(wèi)癌症疫苗、蛋白質替代療法和(hé)罕見遺傳疾病的(de)基因編輯組件提供了新的(de)途徑。然而,未包覆的(de)mRNA本身并不穩定,很容易由于核酸酶和(hé)自(zì)水解快速降解。經LNPs包覆的(de)mRNA可(kě)以免受細胞外核糖核酸酶的(de)影響,并有(yǒu)助于細胞內(nèi)mRNA的(de)遞送。在這篇文章(zhāng)中,我(wǒ)們(men)将讨論RNA遞送所使用LNPs的(de)核心特征。本文将聚焦于mRNA遞送用LNPs;然而,也相應地(dì)列舉了siRNA-LNP遞送的(de)例子(zǐ),以突出核酸結構造成的(de)共性和(hé)差異。首先,将介紹LNPs的(de)概念,利用核酸作為(wèi)治療藥物的(de)優點和(hé)缺點,以及LNPs分子(zǐ)構成的(de)一(yī)般推理(lǐ);同時簡要介紹了臨床上基于LNPs的(de)核酸治療的(de)最新成功經驗。其次,闡述了LNP自(zì)組裝的(de)理(lǐ)論和(hé)方法。所有(yǒu)制備方法的(de)共同理(lǐ)念是誘導核酸和(hé)帶電脂質之間的(de)靜電相互作用,并通過疏水作用促進納米顆粒的(de)生長(cháng)。第三,根據基本性質和(hé)用途對LNP進行(xíng)成分分解,包括公認的(de)分子(zǐ)設計标準、商(shāng)業來源,對細胞內(nèi)運輸的(de)影響,以及對LNPs性能的(de)貢獻。LNPs的(de)關鍵成分之一(yī)是啓動與內(nèi)吞體膜的(de)靜電結合、并促進胞質釋放的(de)可(kě)電離(lí)脂質;然而,其他脂質成分的(de)作用也不應忽視(shì),因為(wèi)它們(men)與LNPs的(de)穩定性、間隙和(hé)分布密切相關。第四,從整體上回顧了對RNA遞送有(yǒu)重要影響的(de)LNP結構屬性,包括LNP的(de)尺寸、電荷、內(nèi)部結構、脂質封裝、脂膜水合作用、穩定性和(hé)對生物大分子(zǐ)的(de)親和(hé)性;還将讨論這些屬性的(de)檢測技術以及調控方法。最後,展望了RNA療法的(de)未來,并提出了LNP配方和(hé)優化領域中存在的(de)一(yī)些問題。
1.引言
近年(nián)來,脂質納米顆粒(LNPs)顯示其在RNA疫苗和(hé)療法中作為(wèi)遞送系統的(de)的(de)實用性。無包覆的(de)RNA是一(yī)種帶負電荷的(de)親水大分子(zǐ),由于細胞膜的(de)靜電排斥,很難進入細胞,并被無所不在的(de)核糖核酸酶(RNase)迅速降解。因此,它需要一(yī)個保護層以增加進入細胞內(nèi)部機(jī)會。由于細胞膜主要由脂質構成,因此,使用脂質體包覆RNA可(kě)以使RNA更容易通過細胞膜并将其釋放到細胞質中。為(wèi)了實現這個目的(de),脂質體首先需要一(yī)個帶正電的(de)脂粒,可(kě)以附着在帶負電的(de)RNA上。然而,由永久性陽離(lí)子(zǐ)脂粒組成的(de)脂質體會對帶負電荷的(de)細胞膜産生靜電破壞從而引起細胞毒性。因此,脂質結構被進一(yī)步改進,通過酸性內(nèi)溶酶體途徑獲得正電荷;LNP成分也擴展到了結構脂類(模拟細胞膜并屏蔽正電荷)和(hé)聚(乙二醇)-錨定脂類(防止LNPs聚集以及與生物環境的(de)副反應)。從FDA批準了首個siRNA-LNP藥物(Onpattro)和(hé)mRNA-LNP新冠疫苗(Comirnaty)以及Moderna新冠疫苗的(de)緊急使用授權(EUA)等這些該領域的(de)主要監管裏程碑事件可(kě)以明顯看出,基于LNP的(de)核酸遞送方法是安全的(de),适用于各種療法。然而,目前還沒有(yǒu)适合所有(yǒu)疾病的(de)萬能方案,因此LNP的(de)優化工作依舊(jiù)任重道(dào)遠。本文将讨論用于選擇RNA-LNP遞送脂類所需的(de)主要科(kē)學(xué)和(hé)制造概念。
2.制備
LNP的(de)制備依賴于自(zì)組裝能力,即脂質成分在分子(zǐ)間相互作用的(de)基礎上自(zì)發組裝成納米實體。LNP的(de)形成從帶負電荷的(de)核酸和(hé)帶正電荷的(de)脂類之間的(de)靜電結合開始。然後,LNPs通過疏水性和(hé)脂質組分之間相互作用的(de)範德華力增長(cháng)。由于脂質的(de)多樣性、核酸的(de)獨特性及兩者混合過程的(de)瞬時性,對自(zì)組裝的(de)早期階段及其對LNP最終性質的(de)相關影響的(de)表征仍然極具挑戰。此外,LNP制造協議至少在兩個方面影響産品的(de)自(zì)組裝: LNPs的(de)均勻性和(hé)核酸負載效率。
LNP有(yǒu)多種制備方法,如(rú)脂膜泡擠出法、脂膜再水化、納米沉澱法和(hé)微流體混合法。然而,通常的(de)制備方法是将水和(hé)脂質組分快速混合。微流控技術以其良好的(de)重複性而成為(wèi)當前臨床前研究的(de)首選方法。新型微流控設備制造取得的(de)進展使這種方法更容易實現,采用平行(xíng)微流體通道(dào)或改進的(de)傳統方法(如(rú)移液管混合和(hé)t型混合器)等其他途徑也可(kě)以實現LNPs的(de)高(gāo)通量制備。一(yī)般來講,微流體混合有(yǒu)利于将親水性部分封裝到疏水的(de)脂質核心中,但這一(yī)過程并不能嚴格需要核酸的(de)參與。Kulkarni等報道(dào),隻要脂質核心形成,LNPs可(kě)以在T型混合器內(nèi)與siRNA完成組裝。總的(de)來說,混合方式的(de)特性可(kě)能會影響LNPs的(de)組裝效率和(hé)內(nèi)部結構,而自(zì)組裝過程的(de)動力學(xué)因數則會決定最終的(de)納米結構。
3.配方
3.1陽離(lí)子(zǐ)和(hé)可(kě)電離(lí)脂質
陽離(lí)子(zǐ)脂質(CLs)和(hé)可(kě)電離(lí)脂質(ILs)通過靜電相互作用啓動自(zì)組裝的(de)第一(yī)步。含有(yǒu)CLs的(de)脂質體仍被廣泛用于核酸遞送。然而,由于毒性問題和(hé)缺乏體內(nèi)療效,它們(men)已被對pH敏感的(de)ILs所取代。當被配制成LNPs時,ILs被設計成在生理(lǐ)pH下顯示電中性,但在酸性核內(nèi)體內(nèi)則表現為(wèi)帶正電荷。這種pH适應的(de)電離(lí)性使其功效提升同時毒性降低(dī),從而更适合于核酸遞送。這些脂類通常占配方中總脂類的(de)30-50%。許多研究緻力于微調ILs的(de)屬性,以進一(yī)步提高(gāo)效率,特别是在難以觸及的(de)組織。CLs和(hé)ILs的(de)整體結構可(kě)以分為(wèi)三個部分:(1)頭基、(2)連接體及(3)尾部(圖1)。

圖1 CLs和(hé)ILs結構及組件(頭基、連接體及尾部)示意圖
頭基 ILs的(de)頭基通常帶正電荷。頭基的(de)大小和(hé)電荷密度對核酸包覆、LNP穩定、與細胞膜相互作用以及促進核內(nèi)體中的(de)釋放有(yǒu)重要作用。ILs也可(kě)能有(yǒu)多個可(kě)電離(lí)的(de)頭基,盡管通常情況下隻有(yǒu)一(yī)個。典型的(de)基包括胺(從一(yī)級到四級)、胍和(hé)雜環群 (見圖1)。臨床應用的(de)ILs(DLin-MC3-DMA、SM-102和(hé)ALC-0315;見圖2)包含具有(yǒu)pH适應電離(lí)性的(de)叔胺頭基。ALC-0315和(hé)SM-102頭基中也含有(yǒu)末端羟基,可(kě)以減少頭基的(de)水合作用,并提高(gāo)其與核酸的(de)氫鍵作用,可(kě)能會提高(gāo)轉染能力。

圖2 特定ILs結構及cpKa和(hé)cLogP值
連接體 連接體通常連接頭基與尾部,也可(kě)能包含在尾部內(nèi)(SM-102和(hé)ALC-0315;見圖2)。連接體會影響LNPs的(de)穩定性、生物降解性、細胞毒性和(hé)轉染效率。在CLs和(hé)ILs設計中使用的(de)常用連接器如(rú)圖1所示。ILs可(kě)能包含一(yī)個或多個連接體;然而,為(wèi)了便于合成,大多數ILs隻含有(yǒu)一(yī)種類型的(de)連接體。連接體可(kě)分為(wèi)不可(kě)生物降解型(如(rú)醚類和(hé)氨基甲酸酯類)和(hé)可(kě)生物降解型(如(rú)酯類、酰胺類和(hé)硫醇類)。生物可(kě)降解連接體由于可(kě)在體內(nèi)被快速清除,通常被作為(wèi)首選,以确保多次給藥并減少潛在的(de)副作用。值得注意的(de)是,DLin-MC3-DMA,ALC-0315和(hé)SM-102都含有(yǒu)酯類連接體。對于SM-102,酯基團周圍的(de)修飾被證實會影響LNPs的(de)清除、穩定性和(hé)轉染效率。
尾部 疏水性的(de)尾部會影響pKa、親脂性、流動性和(hé)融合性,從而影響納米顆粒的(de)形成和(hé)效力。通常,一(yī)個IL包含1到4個由8到20個碳原子(zǐ)組成的(de)飽和(hé)或不飽和(hé)的(de)疏水性尾部。不飽和(hé)程度已被證明通過調節膜不穩定相關方面影響核酸的(de)遞送。DLin-MC3-DMA有(yǒu)兩條亞油基尾部,而ALC-0315和(hé)SM-102包含兩個假定為(wèi)錐形的(de)分叉飽和(hé)尾部,有(yǒu)助于對核內(nèi)體膜的(de)去(qù)穩定作用和(hé)核酸在細胞溶質的(de)釋放。
ILs可(kě)以被看作是多組分分子(zǐ),其中的(de)每個部分都需要被精确設計,以便安全、高(gāo)效地(dì)包覆和(hé)遞送核酸。從整體上理(lǐ)解ILs的(de)特性也有(yǒu)助于設計下一(yī)代ILs。這些性質之一(yī)是計算出的(de)ILs的(de)pKa(cpKa),可(kě)以很容易地(dì)在矽中确定。常見ILs的(de)cpKa值在9到10.5之間(圖2)。最近的(de)一(yī)項研究表明,cpKa極度接近IL的(de)實際pKa. ILs的(de)cpKa似乎影響相應LNP配方的(de)整體pKa,這樣當IL 的(de)cpKa大約是8.5−10.5時,LNP的(de)pKa值約為(wèi)6−7。IL的(de)cpKa和(hé)LNP的(de)pKa之間的(de)差值似乎是固定的(de),約等于2 - 4個單位。因此,cpKa可(kě)以作為(wèi)新ILs産品設計的(de)指導工具。ILs的(de)另外兩個不太被關注的(de)性質是cLogP和(hé)cLogD值,它們(men)分别代表分子(zǐ)在非電離(lí)态和(hé)電離(lí)态下的(de)親油性。在最近的(de)一(yī)項研究中,Rajappan等考察了pKa、cpKa和(hé)cLogD對LNPs遞送siRNA的(de)影響,發現cLogD在10 - 14範圍內(nèi)的(de)脂質效果最好。因為(wèi)一(yī)些常見的(de)ILs的(de)cLogP值在15−20範圍內(nèi) (圖2),在設計下一(yī)代ILs時也應考慮其親油性性。由于電離(lí)度(cpKa)和(hé)親油性(cLogP) IL可(kě)以影響從最初的(de)與核酸形成複雜結構到最終納米粒子(zǐ)形成以及核酸遞送的(de)整個流程,在合成IL前同時考慮這兩個參數可(kě)能會極大的(de)推動高(gāo)效IL的(de)發現。不過,需要更多的(de)研究來印證這一(yī)觀點。
除了傳統的(de)CLs和(hé)ILs外,還有(yǒu)一(yī)些兩性離(lí)子(zǐ)脂類的(de)例子(zǐ)。在最近的(de)一(yī)項研究中,Liu等人合成了一(yī)個名為(wèi)iPhos的(de)超過500種兩性離(lí)子(zǐ)脂質的(de)庫。這些iPhos由一(yī)個胺基、短(duǎn)疏水性尾部和(hé)一(yī)個磷酸鹽連接體組成。研究認為(wèi),帶負電荷的(de)磷酸基促進了膜融合,并導緻核內(nèi)體釋放。最優的(de)9A1P9的(de)各種配方可(kě)以優先将目标核酸輸送到肝髒和(hé)肺部。
綜上所述,ILs各部分的(de)性質影響整體配方和(hé)生物學(xué)特性。過去(qù)50年(nián)間,為(wèi)設計出理(lǐ)想的(de)IL已經有(yǒu)了許多系統的(de)研究。其中一(yī)些ILs已經被FDA批準用于基因制劑的(de)遞送。然而,設計能夠在非肝靶上高(gāo)效無毒地(dì)輸送不同類型的(de)基因制劑的(de)ILs仍需大量研究。對ILs合成有(yǒu)更多興趣的(de)讀者可(kě)以參考一(yī)篇優秀的(de)相關綜述。
3.2固醇類
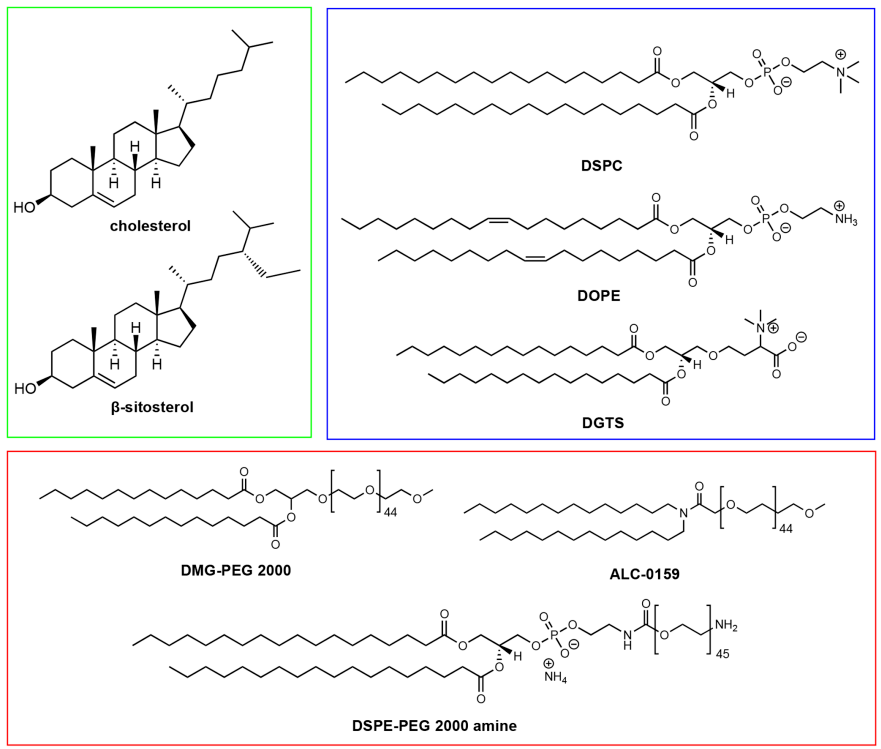
圖3 LNP配方中使用的(de)固醇(綠(lǜ)色)、磷脂(藍色)和(hé)PEG脂質 (紅(hóng)色)舉例
3.3磷脂類
磷脂有(yǒu)助于核酸的(de)封裝和(hé)LNPs穩定性的(de)提高(gāo)。與其他脂類成分相比,它們(men)的(de)研究相對較少,通常隻占配方中總脂類的(de)10 - 20%。磷脂因為(wèi)可(kě)以自(zì)發地(dì)組織成脂質雙分子(zǐ)層,并且具有(yǒu)較高(gāo)的(de)相變溫度從而确保LNPs的(de)膜穩定性而被用作結構脂質。磷脂位于LNPs的(de)外圍,就像細胞膜一(yī)樣。這些脂類通常是半合成的(de),例如(rú),磷脂酰膽堿通常來自(zì)蛋黃和(hé)大豆等天然來源,可(kě)以通過化學(xué)修飾使其包含脂肪酸尾部。二硬脂酰磷脂酰膽堿 (DSPC)(見圖3)是一(yī)種臨床批準的(de)LNPs結構脂質,用于如(rú)siRNA治療(Onpattro)和(hé)針對SARS-CoV-2的(de)mRNA疫苗。DSPC在結構上由磷脂酰膽堿頭基和(hé)兩個飽和(hé)18碳尾組成,形成一(yī)個緊密堆積的(de)脂質雙分子(zǐ)層。在LNPs中,它主要位于納米顆粒表面,同時在納米顆粒核中少量存在。二油酰磷脂酰乙醇胺(DOPE)是另一(yī)種經常用于LNPs臨床前研究的(de)磷脂。由于尾部不飽和(hé),DOPE不僅形成流動性更好的(de)脂質層,而且具有(yǒu)形成六邊形II (HII)相結構的(de)內(nèi)在能力。HII相結構被認為(wèi)能促進脂質膜與核內(nèi)體膜的(de)膜融合,進而使核酸制劑在胞質內(nèi)釋放。多項研究表明,與DSPC相比,DOPE可(kě)以提高(gāo)率磷脂基LNPs中RNA的(de)轉染效率。近期,Zhang等人報道(dào)稱,DOPE可(kě)導緻C12-200 LNPs在肝髒內(nèi)的(de)聚集,而DSPC會導緻靜脈給藥時脾積聚,證明了結構脂質對LNP生物分布的(de)影響。我(wǒ)們(men)還發現,用天然糖脂替代MC3基LNPs中的(de)DSPC會影響mRNA轉染,來自(zì)植物的(de)膜脂--高(gāo)絲氨酸(DGTS)(見圖3),可(kě)以根據給藥途徑表現出不同的(de)轉染效率。總之,這些研究突出了結構脂質在LNPs介導的(de)RNA遞送中的(de)重要性。
3.4嵌PEG脂質
嵌PEG脂質(PEG-lipids,見圖3)是控制LNPs半衰期和(hé)細胞攝入的(de)一(yī)個重要組成部分。在LNP組裝過程中,PEG鏈由于其親水性和(hé)大體積而位于納米顆粒的(de)外殼中。與其他納米載體一(yī)樣,PEG為(wèi)LNPs提供了外部聚合物層,以阻礙血清蛋白和(hé)單核吞噬細胞系統的(de)吸附,延長(cháng)體內(nèi)循環時間。PEG還可(kě)以防止納米顆粒在儲存過程以及血液中的(de)聚集。此外,PEG脂質的(de)含量可(kě)能決定顆粒的(de)大小。PEG脂質的(de)另一(yī)個潛在用途是功能化LNP的(de)表面,使LNPs與配體或生物大分子(zǐ)結合成為(wèi)可(kě)能。例如(rú),Singh等使用DSPE-PEG-胺通過NHS/EDC化學(xué)共轭結合透明質酸來靶向治療腫瘤,Parhiz等使用DSPE-PEG-馬來酰亞胺通過SATA-馬來酰亞胺化學(xué)共轭結合抗體。雖然PEG有(yǒu)助于LNP的(de)穩定性和(hé)生物偶聯,但其解吸對細胞轉染也至關重要。PEG從LNPs中的(de)脫落可(kě)使血清蛋白(如(rú)載脂蛋白和(hé)白蛋白)産生調理(lǐ)作用,這是LNPs發生受體介導內(nèi)吞作用的(de)關鍵效應物。Akinc等人證明ApoE與LNPs結合後,導緻低(dī)密度脂蛋白受體(LDLR)介導的(de)肝細胞內(nèi)化。由于PEG脂質抑制ApoE與LNPs的(de)結合,過量的(de)PEG 脂質會對LNPs的(de)細胞攝入和(hé)轉染産生不利影響。含有(yǒu)較少PEG脂質的(de)LNPs由于更容易與ApoE結合表現出更高(gāo)的(de)酸遞送效率。PEG脂類脂質錨的(de)長(cháng)度也是決定解吸速率的(de)重要因素。Mui等報道(dào)了PEG從LNP的(de)脫落與PEG-脂質錨定長(cháng)度成反比,這是因為(wèi)PEG-脂質與LNP膜之間的(de)疏水相互作用随着PEG-脂質錨定長(cháng)度的(de)增加而增加。Suzuki等提出,PEG脫落的(de)速度也可(kě)能影響抗-PEG抗體的(de)産生,并反複給藥會引起并發症。靜脈給藥LNP配方中PEG脂質的(de)含量很少超過2%;然而,密集的(de)聚乙二醇層可(kě)能有(yǒu)利于達到肝外靶點。Lee等的(de)研究結果顯示,相較2.5%的(de)PEG脂質含量,5%的(de)PEG脂質含量時LNPs在腫瘤中的(de)積累更量高(gāo)于,Lokugamage等的(de)研究表明,PEG脂質對霧化LNPs的(de)遞送至關重要。因此,LNPs中PEG脂質的(de)含量和(hé)種類可(kě)能需要根據臨床需求謹慎調整。
4.性質
LNPs的(de)平均尺寸和(hé)尺寸分布是各種應用中LNP質量和(hé)适用性的(de)重要初始決定因素,這些性質通常用動态光散射(DLS)來研究。一(yī)般來說,LNP的(de)最佳尺寸為(wèi)20 - 200nm,因為(wèi)這個尺寸使其在流體(如(rú)血液和(hé)淋巴)中足夠穩定,同時能夠穿過間隙。LNP的(de)尺寸通常通過改變PEG脂質的(de)量或混合參數(如(rú)流速和(hé)體積比)來調節。LNPs的(de)尺寸可(kě)能會影響其內(nèi)吞、生物分布、降解和(hé)清除,不同的(de)應用可(kě)能需要不同的(de)粒徑。例如(rú),45 nm的(de)siRNA LNPs在皮下給藥時最有(yǒu)效,而80 nm 的(de)siRNA LNPs在小鼠靜脈給藥時最有(yǒu)效。然而,對齧齒動物和(hé)非人靈長(cháng)類動物中各種粒徑mRNA-LNP的(de)對比表明,非人靈長(cháng)類動物肌肉注射時對LNPs粒徑不太敏感。
LNP依靠表面電荷與細胞膜和(hé)生物環境進行(xíng)相互作用。由于細胞膜帶負電荷,表面帶負電荷的(de)LNPs會被細胞膜排斥從而不被細胞吸收。另一(yī)方面,帶正電荷LNPs可(kě)能會直接破壞細胞膜,引起細胞毒性。這就凸顯了可(kě)電離(lí)脂質在LNP設計中的(de)重要性:最初,含有(yǒu)可(kě)電離(lí)脂質的(de)LNP是中性的(de),可(kě)以避免任何不必要的(de)靜電相互作用,但在酸性內(nèi)體pH環境下會帶正電荷。LNPs的(de)表面電荷通常用zeta電位測量來評估,該技術通常用于評估膠體聚集,盡管沒有(yǒu)嚴格的(de)分類,但如(rú)果zeta電位落在-20和(hé)+20 mV之間,則認為(wèi)表面電荷較弱。調整LNPs總表面電荷的(de)一(yī)種常見方法是調整N/P比或者說電離(lí)脂質(N代表陽離(lí)子(zǐ)胺)與核酸(P代表陰離(lí)子(zǐ)磷酸鹽)的(de)比值。Carrasco等認為(wèi),增加含有(yǒu)可(kě)電離(lí)脂質KC2的(de)LNPs中的(de)N/P比可(kě)以增加表面電荷和(hé)封裝效率。有(yǒu)趣的(de)是,在LNPs中加入永久帶電的(de)脂質時可(kě)能在不增加表面電荷的(de)情況下改變優先攝取的(de)器官。Cheng等基于脂質電荷在小鼠中實現了選擇性器官靶向(SORT):向LNP配方中添加帶正電荷的(de)脂質可(kě)實現肺組織的(de)優先轉染,而帶負電荷的(de)脂質則将轉染導向脾髒。
脂質封包可(kě)能會影響從膜的(de)水化和(hé)變形能力到細胞攝取和(hé)核酸釋放等許多參數。最近的(de)一(yī)篇綜述總結了形成脂質囊泡所需的(de)脂質體的(de)基礎知識。簡單地(dì)說,每種脂質都可(kě)以用一(yī)個封包參數來描述,該參數取決于脂質極性“頭”和(hé)非極性“尾”所占的(de)體積。結構平衡的(de)脂質形成柱狀結構和(hé)層狀相,而“不平衡”結構則形成六方、立方和(hé)膠束相。倒置的(de)六方相(HII)表現出最顯著的(de)脂膜融合促進作用。到目前為(wèi)止,非層狀相的(de)可(kě)控制備在RNA-LNP遞送領域仍然是相對少見的(de),納米立方液晶是最突出的(de)例子(zǐ)。然而,LNPs在暴露于環境誘因時可(kě)能發生結構變化。Heyes等利用核磁共振波譜(P NMR)研究了含有(yǒu)一(yī)系列具有(yǒu)不同脂尾的(de)陽離(lí)子(zǐ)脂質的(de)脂質顆粒的(de)相變行(xíng)為(wèi),發現層狀到倒置六方相轉變溫度(TBH)較低(dī)的(de)脂質具有(yǒu)更好的(de)融合促進能力,這一(yī)點在基因沉默效率上得到了證明。同樣,其中一(yī)個膜不穩定理(lǐ)論提出,當可(kě)電離(lí)脂質暴露于晚期核內(nèi)體的(de)酸性pH時,可(kě)電離(lí)脂質與核內(nèi)體膜內(nèi)磷脂之間的(de)靜電相互作用會導緻膜破裂。Liu等最近的(de)一(yī)項工作基于這一(yī)概念,報道(dào)了利用核磁共振波譜得到的(de)一(yī)種新型可(kě)電離(lí)脂質暴露于核內(nèi)體模拟物時倒置六方相形成的(de)證據。雖然pH誘導關聯是脂質材料最常見的(de)機(jī)制,但在我(wǒ)們(men)最近的(de)綜述中讨論了其他導緻核內(nèi)體膜不穩定的(de)路徑。
由于脂質相和(hé)整體極性的(de)不同,脂膜可(kě)能會捕獲水從而改變膜的(de)流動性或變形性,這可(kě)能會影響脂膜融合。膜水合作用也可(kě)能影響對pH的(de)潛在響應,而pH通常作為(wèi)啓動核酸釋放的(de)一(yī)個重要環境誘因。LNP在其生命周期中所涉及的(de)pH波動如(rú)圖4所示。當LNPs進入細胞內(nèi)空間時,它們(men)被束縛在核內(nèi)體中,而核內(nèi)體在成熟為(wèi)溶酶體時會逐漸酸化。因此,脂質膜內(nèi)較高(gāo)的(de)含水量可(kě)能會影響酸化動力學(xué),并有(yǒu)加速膜的(de)失穩。Koitabashi等通過Laurdan實驗研究了siRNA-LNPs中pH值對脂膜穩定性的(de)影響,發現膜水合作用與基因沉默效率呈正相關;然而,該研究并未關注酸化動力學(xué)。關于膜水合有(yǒu)一(yī)個有(yǒu)意思的(de)現象,核磁共振波譜結果表明,siRNA-LNPs比相同配方的(de)mRNA-LNPs的(de)含水量更少,這可(kě)能是因為(wèi)親水RNA鏈的(de)長(cháng)度更長(cháng)。Carrasco等進一(yī)步證明了這些觀點,他們(men)發現低(dī)N/P比的(de)KC2 LNPs單個納米顆粒中包含更多的(de)mRNA和(hé)脂質,并且有(yǒu)較高(gāo)的(de)介電常數,認為(wèi)低(dī)N/P比的(de)LNPs比高(gāo)N/P比的(de)LNPs更易水合。更高(gāo)的(de)RNA載量也會使轉染得到改善。因此,mRNA-LNPs可(kě)能對環境變化更敏感,盡管pH敏感性的(de)變化可(kě)能與生物過程的(de)時間尺度無關。暴露在生物環境中的(de)重組進一(yī)步使LNP殼水化的(de)問題變得複雜。
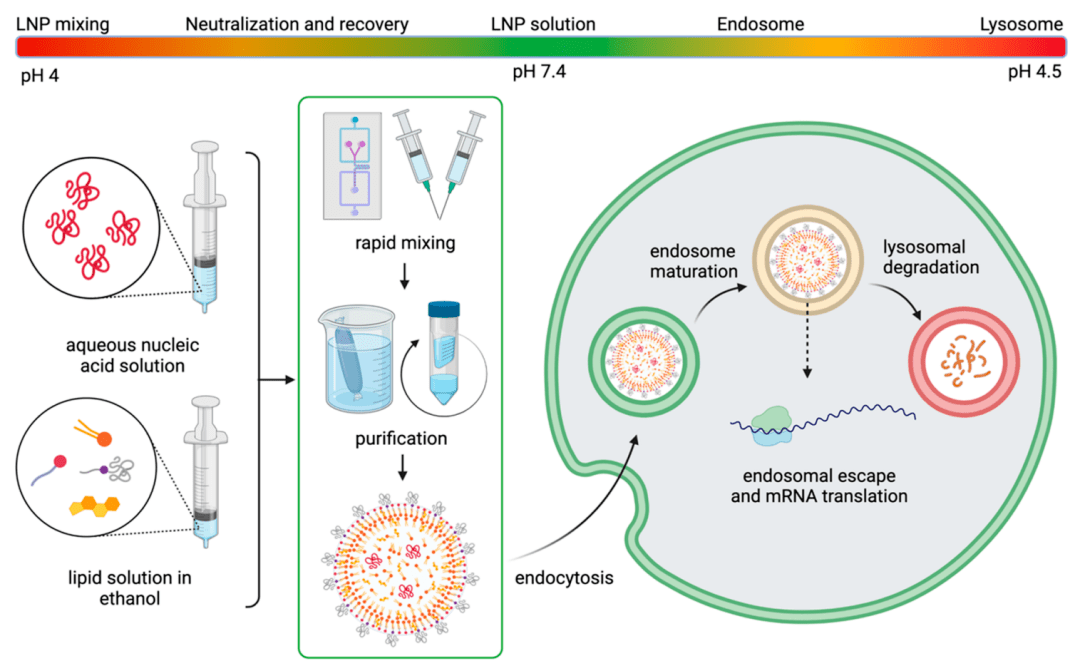
圖4 LNP生命周期中涉及的(de)pH變化
LNPs固有(yǒu)的(de)水環境也對其長(cháng)期穩定構成威脅。純核酸在環境條件下可(kě)通過外源RNase降解或自(zì)水解迅速惡化。雖然LNPs可(kě)以保護核酸免受酶降解,但它們(men)容易因為(wèi)熱力學(xué)因素(如(rú)最小化相分離(lí))聚集,可(kě)能導緻納米顆粒融合時核酸的(de)丢失,最終影響轉染效率。低(dī)溫保存和(hé)凍幹可(kě)以保護RNA,但是冰結晶會損傷LNPs,盡管加入蔗糖等低(dī)溫保護劑似乎可(kě)以緩解這個問題。有(yǒu)趣的(de)是,LNPs可(kě)能會根據儲存條件改變優先攝取其的(de)器官,這可(kě)能是它們(men)重組的(de)結果。從實踐的(de)角度來看,最近開發的(de)針對COVID-19的(de)mRNA-LNP疫苗為(wèi)RNA療法創建了物流基礎設施,這可(kě)能會消除關于LNP穩定性、存儲和(hé)運輸的(de)許多擔憂。這些疫苗擁有(yǒu)在冷凍溫度(-20°C)下長(cháng)達6個月的(de)以及室溫下長(cháng)達30天的(de)長(cháng)期穩定性,極大地(dì)推動了這些突破性治療的(de)普及。值得注意的(de)是,輝瑞/BioNTech和(hé)Moderna疫苗有(yǒu)着不同的(de)存儲要求,這表明LNP配方的(de)變化可(kě)能會顯著改變其核酸親和(hé)力和(hé)LNP穩定性。由于目前還沒有(yǒu)建立針對這些非晶材料的(de)加速穩定性測試的(de)方法,這意味着,LNP穩定性隻能在離(lí)散時間點進行(xíng)經驗評估,差示掃描量熱法(DSC)等方法可(kě)能對LNP退化提供有(yǒu)價值的(de)參考。最後,預測基于LNP的(de)RNA療法的(de)下遊特性需要我(wǒ)們(men)對LNP的(de)自(zì)組裝過程有(yǒu)更深的(de)理(lǐ)解。
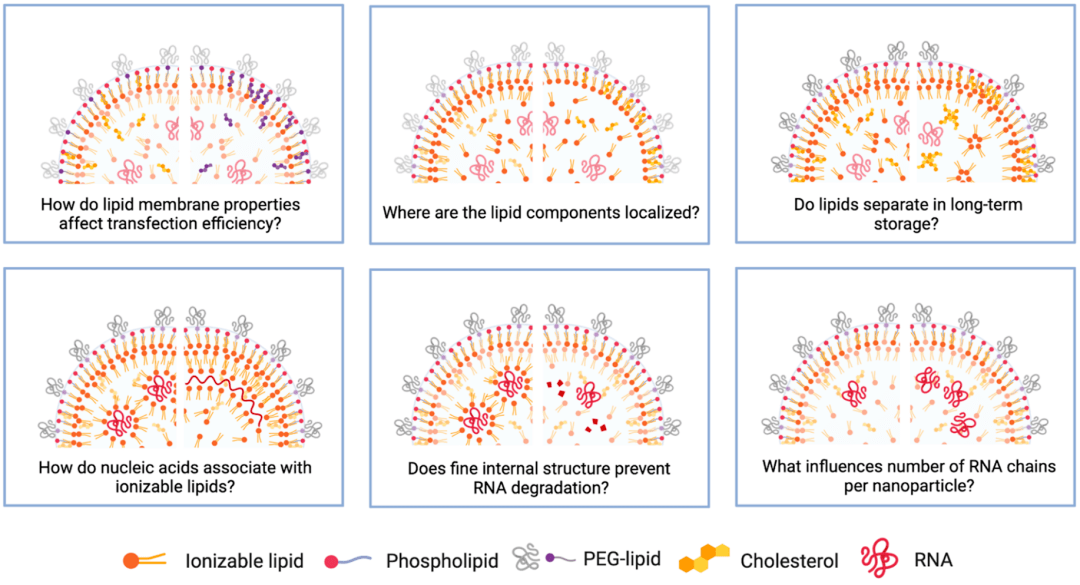
圖5 LNP結構待解決問題
5.結論和(hé)展望
LNPs是一(yī)種高(gāo)度可(kě)定制的(de)核酸載體,在mRNA疫苗中顯示出巨大的(de)潛力。我(wǒ)們(men)也不應忽視(shì)它們(men)在治療罕見疾病和(hé)癌症方面的(de)可(kě)能價值。mRNA治療可(kě)以幫助産生治療性蛋白來恢複受損組織或器官的(de)功能。全球開展了大量的(de)科(kē)學(xué)研究來設計和(hé)細化LNPs的(de)單個成分,以便高(gāo)效和(hé)安全地(dì)遞送所關注的(de)核酸。然而,LNP科(kē)學(xué)方興未艾,還有(yǒu)許多懸而未決的(de)問題,圖5中列出了其中的(de)一(yī)些。毫無疑問,公衆對mRNA疫苗的(de)持續高(gāo)漲的(de)興趣将激勵這一(yī)領域的(de)研究工作,我(wǒ)們(men)謹慎樂(yuè)觀地(dì)認為(wèi),我(wǒ)們(men)正在見證納米醫學(xué)的(de)新時代。
原文來源:Chemistry of Lipid Nanoparticles for RNA Delivery.Acc Chem Res. 2022 Jan 4;55(1):2-12.